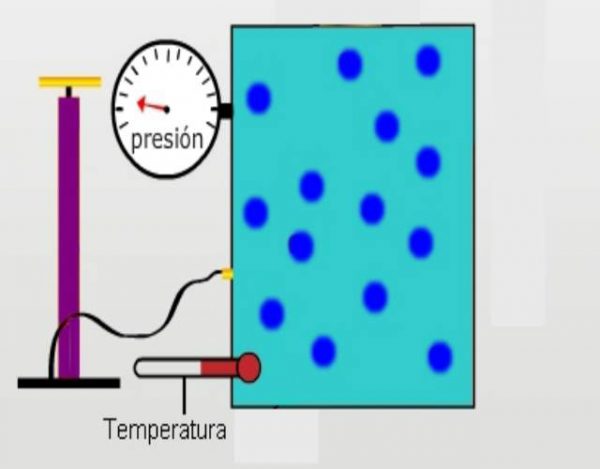
En la actualidad muchos no conocen la teoría sobre el comportamiento de los gases. Estas leyes fueron desarrolladas por Boyle, Charles y Gay Lussac. Estos científicos diferenciaron y conceptualizaron los parámetros de relación entre volumen, presión y temperatura de un gas.
Dichas observaciones están basadas de forma macroscópica del campo empírico. No obstante, existen otras formas de explicar el comportamiento de un gas. La teoría atómica es una de ellas, quien considera que todas estas sustancias están compuestas por un gran número de partículas. Entre las que destacan los átomos y las moléculas.
En primer lugar todas las observaciones de un gas arrojan a resultados directos sobre su composición, presión, temperatura y volumen. La teoría cinética molecular consta de 5 grandes conceptos. Todas son singulares, pero que complementan el comportamiento del gas. Todos estos conceptos están basados en principios básicos que involucran la química y la física. No obstante algunas de ellas incluyen conceptos futuristas o proyecciones para darle un mejor campo de explicación.
Conceptos de la teoría cinética molecular
- El gas está compuesto de pequeñas partículas que se mueven de forma rectilínea. Aquí entra el concepto de la ley de Newton.
- Es extraño, pero, las moléculas de un gas no ocupan espacio.
- El contacto entre dichas moléculas es totalmente elástico. Esto como consecuencia trae que el contacto no disminuye la energía, ni el movimiento de los participantes. Es como si el choque causara otros contactos moleculares.
- Cuando las moléculas están en movimiento no existe ningún tipo de fuerza, ni de atracción, ni de repulsión.
- La energía cinética en estos casos suele rondar los 3kT/2. La cual T es de temperatura absoluta y la K, la constante de Boltzmann.
Significado de estos conceptos
Estos conceptos son tomados como válidos hoy en día, conocidos como el modelo cinético molecular. Todo gas está compuesto por pequeñas partículas como lo mencionamos antes. Asi mismo se encuentran en total cohesión, para componer el elemento definitivo.

Estos movimientos están llenos de vacío interpuesto, que garantizan el choque elástico, con el fin de mantener la materia. Cuando las moléculas están muy estrechas, estas fuerzas aumentan considerablemente. Es lo que se considera como el estado sólido de la materia. Pero cuando esta composición es más separada, estamos en presencia del estado líquido. Finalmente cuando se encuentran separadas en gran proporción, este comportamiento se presenta en estado gaseoso, donde las fuerzas son mínimas entre sí.